В физике и химии существует такое понятие как твердые тела. Основными свойствами твердых тел являются возможности сохранения объема и формы. По типу внутреннего строения они делятся на кристаллические и аморфные. К первым относятся поваренная соль, металлы, сахар, графит, минералы и т.д., ко вторым – стекло, смолы, пластмассы, воск и т.д. Чем же отличаются аморфные вещества от кристаллических?

Кристаллическое строение отличается упорядоченностью и значительным расстоянием между частицами. Вещества, атомы и молекулы которых расположены более хаотично и на близком расстоянии, называются аморфными. По своему строению они близки к жидкостям.
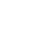
Существует способ визуального определения кристаллических и аморфных тел: на изломе кристаллы имеют плоские грани и ступенчатую поверхность, в то время как аморфные тела образуют поверхность неправильной формы.
Аморфное состояние веществ считается неустойчивым. Многие такие тела со временем могут стать кристаллами. К примеру, расплавленный сахар при застывании приобретает твердое состояние. И наоборот, некоторые тела с кристаллическим строением при нагревании пребывают в аморфном состоянии.

а) кристаллическое вещество б) аморфное вещество
Вещества с аморфным строением имеют одинаковые свойства по различным направлениям межмолекулярных связей. Это свойство называется изотропией. То есть при повышении температуры такие тела получают «текучесть». Однако, в отличие от кристаллических тел, аморфные вещества не имеют фиксированной температуры плавления.
Атомы и молекулы, образующие кристаллическое тело, располагаются в виде разнообразных пространственных решеток, напоминающих геометрические формы. К примеру, монокристалл поваренной соли выглядит как куб, а алмаза – как правильный шестигранник. В естественных природных условиях монокристаллы встречаются редко. Как правило, большинство кристаллических тел состоит из малых, беспорядочно сросшихся между собой, монокристаллов. Такое тело получило название поликристалл.
Монокристаллы зависят от направления ориентации кристаллических граней. Данное свойство называется анизотропией. Поликристаллы же изотропны по своим свойствам, что обусловлено хаотичностью ориентации монокристаллов, из которых они состоят.
Выводы:
- Частицы аморфных веществ не имеют определенного расположения, в то время как молекулы и атомы кристаллов упорядочены.
- В кристаллических веществах частицы расположены на значительном расстоянии друг от друга.
- Аморфные вещества не имеют фиксированной температуры плавления.
- Кристаллические вещества лучше сохраняют форму.
- Аморфные вещества по свойствам близки к жидкостям, кристаллические – к твердым телам.
- Аморфное состояние веществ считается неустойчивым.
- Вещества с аморфным строением характеризуются изотропией, кристаллы - анизотропией.